L’approvisionnement en eau : un défi que le dessalement des eaux contribue déjà à relever. Dans le prolongement d’une histoire ancienne, le procédés par distillation révèle ses limites. D’où le grand intérêt de l’osmose inverse. Nombre de questions se posent encore : quelles sont les consommations énergétiques associées ? Les impacts environnementaux ? L’état du marché et les coûts ?
En l’espace de quelques décennies, l’accès à l’eau est devenu l’un des défis que l’humanité doit relever rapidement. L’eau est pourtant abondante à l’échelle de la planète : les océans sont une réserve inépuisable à condition de séparer le sel et l’eau. D’autres réserves comme les eaux saumâtres trop salées pour être directement consommables sont aussi exploitables. Cet article détaille les différentes techniques déjà utilisées pour le dessalement des eaux et celles qui sont encore au stade de la recherche. Les aspects économiques, qui conditionnent l’accessibilité de ces techniques, sont également exposés, de même que les dimensions énergétiques et environnementales de la question.
1. Une réponse possible à un besoin grandissant
Selon l’Organisation mondiale de la santé, près de 700 millions de personnes, soit une personne sur dix, n’ont toujours pas accès à de l’eau potable en 2015[1]. Plus inquiétant, un rapport des Nations Unies estimait en 2006 que 60% de la population mondiale sera confrontée à des problèmes d’eau à l’horizon 2025[2]. On entend par là que l’accès à une eau de qualité et en quantité suffisante ne sera pas assuré pour la majorité de l’humanité.
Si l’Organisation mondiale de la santé[3] estime que le seuil vital est de cinq litres par jour et par personne, la situation commence à être critique en dessous de 100 litres par jour pour satisfaire les besoins domestiques et quelques besoins collectifs. Au standard des pays développés, la consommation domestique est de l’ordre de 200 litres par jour et par personne (mais 350 litres aux États-Unis !) et entre un et trois mètres cubes par jour si on ajoute les usages collectifs, dont l’agriculture.
Et, pour plusieurs raisons[4], la situation s’aggrave. La population mondiale augmente plus vite que les ressources en eau mobilisables[5], le niveau de vie des pays émergents s’élève et d’une manière générale, la qualité des eaux a tendance à se dégrader. S’il est évident que les régions tropicales particulièrement sèches sont très vulnérables, de nombreux pays en dehors de ces régions sont déjà touchés : Australie, États-Unis, pays du nord du bassin méditerranéen, Inde, Chine, etc.
Pourtant l’eau est abondante sur terre : 70% de la surface du globe est couverte par une réserve de 1,4 milliards de kilomètres cubes d’eau… salée. Rassemblée, cette eau représenterait un cube de plus de 1000 kilomètres de côté (Figure 1). Mais seulement 0,6% de l’eau présente à la surface du globe est directement utilisable et douce. Le reste est contenu dans les océans mais aussi piégé sous forme de glace, à l’état de vapeur d’eau dans l’atmosphère ou reste simplement inaccessible[6]. Par ailleurs, 36 % de la population mondiale vit à moins de 100 kilomètres d’une côte, 11 % à moins de 10 kilomètres et 6 % à moins de 5 kilomètres[7]. Dessaler l’eau de mer – ou des eaux saumâtres moins salées mais impropres à la consommation – pour obtenir de l’eau douce est alors une solution bien séduisante.
2. Une histoire ancienne
L’idée d’extraire de l’eau potable à partir de la mer n’est d’ailleurs pas nouvelle. La nature le fait depuis toujours à travers le cycle naturel de l’eau. Sous l’effet du soleil, les océans s’évaporent, la vapeur d’eau forme des nuages qui provoquent des précipitations de pluie ou de neige dès que les masses d’air humide atteignent des régions plus froides. L’eau des précipitations est pure car le sel contenu dans la mer n’étant pas volatil, seule l’eau s’évapore.
Les marins de l’antiquité confrontés à l’approvisionnement en eau à bord des bateaux avaient déjà imité la nature en faisant bouillir de l’eau de mer pour en extraire de l’eau non salée par condensation de la vapeur produite (Figure 2). Dans Meteorologica, Aristote (384-322 av. J.C.) écrit : « J’ai prouvé expérimentalement que l’eau salée qui s’évapore s’adoucit et que la vapeur condensée ne reforme pas de l’eau de mer. ». Pline l’Ancien (23-79, Histoire Naturelle), Alexandre d’Aphrodise (150-215) et St Basile (329-379, Homélies) semblent avoir été les premiers à décrire des procédés pour rendre l’eau de mer potable[8].
Fig. 2. Eau de mer chauffée pour extraire de l’eau déssalée par condensation de la vapeur [Source : Meteorologica]
Mais il a fallu attendre le 18ème siècle pour qu’on évoque des procédés permettant d’augmenter la production, améliorer la pureté de l’eau ou économiser l’énergie. Et ce n’est qu’au début du 20ème siècle que sont apparus les premiers procédés vraiment industriels de distillation, c’est-à-dire de concentration des solutions et de production d’eau douce par vaporisation puis condensation.
Puis, autour de 1959, un procédé appelé osmose inverse a été mis au point à l’Université de Californie[9] dans le prolongement de la méthode plus ancienne de séparation des sels contenus dans les mélasses (Dubrunfaut, 1853[10]) et des colloïdes (Graham 1854, à l’origine du terme osmose[11]). Il s’agit d’un procédé membranaire : l’eau douce est extraite de l’eau salée à travers une membrane semi-poreuse, en appliquant une pression. Les premières membranes commerciales datent de 1970.
Les procédés de distillation et les procédés membranaires constituent les deux grandes familles de procédés utilisés aujourd’hui à l’échelle industrielle pour le dessalement d’eau de mer. D’autres méthodes pourraient voir le jour mais elles sont encore au stade du laboratoire ou en cours de développement et rien ne dit s’elles seront compétitives par rapport aux procédés déjà bien implantés.
3. Comment fait-on de l’eau douce à partir d’eau salée ?
Le dessalement des eaux concerne bien sûr l’eau de mer mais aussi les eaux saumâtres. Elles se différencient par leur concentration en sels dissous et par leur composition. Pour les océans, l’eau de mer contient en moyenne 35 grammes de sels par litre, constitués à 86% de chlorure de sodium et 13% de carbonate et sulfate de magnésium et de calcium. En proportion bien moindre, 1% au total, on trouve presque toute la classification périodique des éléments ! Mais la salinité des mers est très variable : sept grammes par litre pour la mer Baltique et jusqu’à 270 gramme par litre pour la mer Morte.
Outre le chlorure de sodium, les eaux saumâtres ont une composition très diverse. La concentration totale est très inférieure à celle de la plupart des mers avec une salinité en général inférieure à dix grammes par litre.
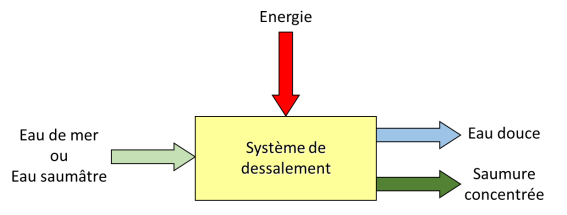
Pour produire de l’eau douce à partir d’eau salée, il faut introduire l’eau brute dans un système auquel on apporte de l’énergie (Figure 3). Il est beaucoup plus facile et avantageux d’extraire l’eau plutôt que le sel : on peut en effet choisir de ne retirer qu’un peu ou beaucoup d’eau, alors qu’il faudrait extraire tout le sel pour obtenir ne serait-ce qu’une goutte d’eau douce. En pratique, pour éviter d’avoir à gérer les 35 kilogrammes de sel contenus dans chaque mètre cube d’eau de mer traitée, on n’extrait pas toute l’eau douce : on préfère concentrer l’eau de mer, d’un facteur environ égal à deux. Ainsi, pour chaque mètre cube d’eau de mer traité – soit 1000 litres – on produira 500 litres d’eau pure et on rejettera une saumure de 500 litres d’eau très salée (contenant 70 grammes par litre de sel).
3.1. Les procédés de distillation et leurs limites
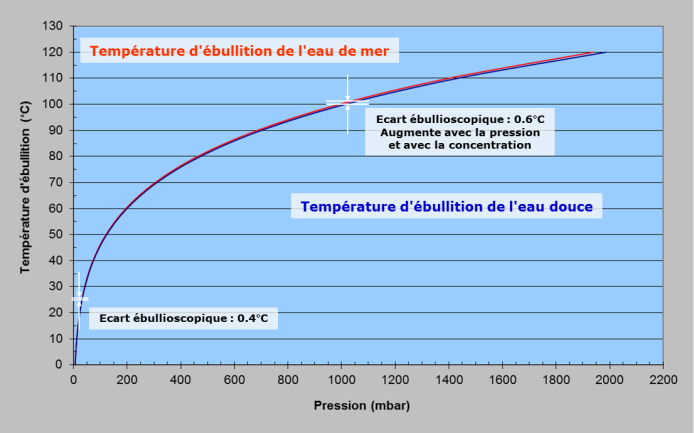
Bien sûr, rien ne parait plus facile que d’imiter la nature. Il suffit de distiller de l’eau de mer pour en extraire de l’eau douce, c’est à dire produire de la vapeur d’eau en faisant bouillir l’eau de mer et récupérer l’eau douce par condensation de la vapeur. Il est à noter qu’à cause de la présence de sel, l’eau salée bout à une température légèrement supérieure à l’eau pure. La différence de température d’ébullition entre l’eau salée et l’eau douce à une pression donnée est appelée écart ébullioscopique.
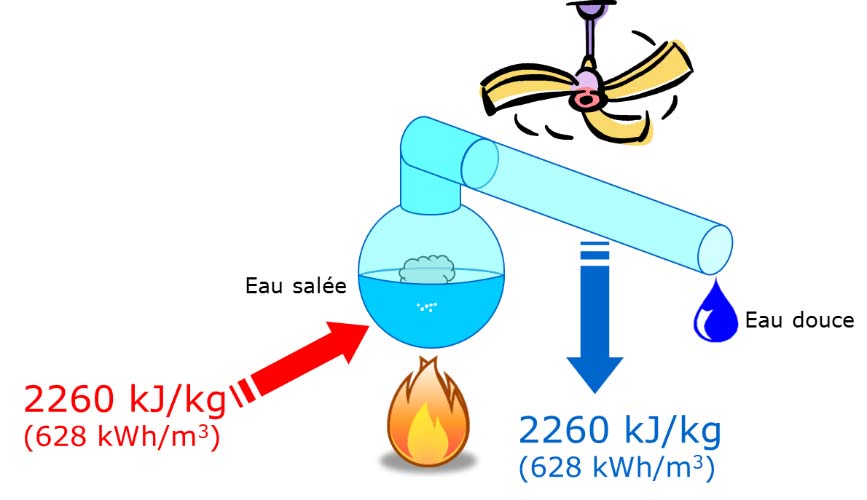 Fig 4 : procédé de distillation – source : auteur
Fig 4 : procédé de distillation – source : auteur
La première difficulté de la distillation est d’ordre économique. Pour évaporer un litre d’eau initialement à 25 degrés, il faut dépenser 2260 kilojoules (kJ) d’énergie. Rien qu’en considérant le coût de l’énergie thermique, sa contribution au prix de l’eau ainsi produite pourrait varier en Europe entre 25 euros par mètre cube (source de chaleur renouvelable biomasse) et 95 euros par mètre cube (source de chaleur électrique)[12]. Ces coûts sont bien sûr déraisonnables pour pouvoir envisager une simple distillation directe[13]. Mais, comme on le verra plus loin, la récupération de chaleur permet d’utiliser la distillation dans des conditions économiques plus acceptables.
Une deuxième difficulté est liée au caractère très corrosif et encrassant de l’eau de mer. L’eau de mer ne contient pas que de l’eau et du sel de cuisine. Elle contient aussi d’autres sels dits à solubilité inverse : plus on les chauffe, moins ils sont solubles. C’est en particulier le cas des carbonates et des sulfates de calcium et de magnésium présents à hauteur de 4,5 grammes par litre. Et l’eau de mer est un milieu « vivant » : elle contient aussi de la matière organique et biologique. Sans précaution particulière, un bouilleur permettant d’évaporer de l’eau de mer va se corroder, s’entartrer, s’encrasser. Mais là encore, les ingénieurs ont trouvé des solutions pour limiter et maîtriser ces phénomènes.
3.2. La révolution du procédé membranaire de l’osmose inverse
L’osmose inverse (Figure 5), industrialisée à partir des années 70 allait révolutionner le dessalement. À nouveau, c’est la nature qui a inspiré les ingénieurs.
L’osmose est un mécanisme naturel d’échange présent dans tous les organismes vivants au niveau des cellules. Sous l’effet d’un écart de concentration, les molécules diffusent des régions les plus concentrées vers les moins concentrées, y compris à travers de fines membranes, comme celles des cellules, si leur nature physico-chimique le permet. Si ce n’est pas le cas, c’est l’eau qui va migrer à travers la membrane pour diluer la zone concentrée et équilibrer les concentrations. À l’équilibre, la différence de pression est appelée pression osmotique.
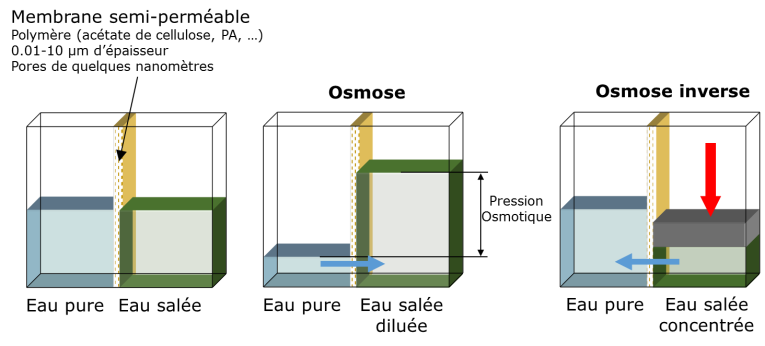 Fig 5 : procédés d’osmose et d’osmose inverse – source : auteur
Fig 5 : procédés d’osmose et d’osmose inverse – source : auteur
L’osmose inverse, qui est au contraire un procédé de séparation, est exactement le phénomène inverse : en appliquant une pression suffisante, on force l’eau à quitter la zone concentrée pour rejoindre la zone à faible concentration. La membrane séparatrice doit bien évidemment avoir la capacité de laisser passer les molécules d’eau tout en arrêtant le sel. La pression à exercer dépend de la concentration en sel et sert à empêcher l’eau pure de retourner diluer l’eau salée… par phénomène d’osmose. On comprend aisément que la pression minimale à appliquer est au moins égale à la pression osmotique, qui correspond juste à l’état d’équilibre. Si on considère l’eau de mer, la valeur de la pression osmotique est environ 29 105 Pascals (Pa), soit près de 30 fois la pression atmosphérique. Pratiquement, pour obtenir un flux significatif et vaincre la pression osmotique qui augmente au fur et à mesure que l’eau est extraite, la pression de travail varie entre 60 et 70 105 Pa.
3.3. Les types de procédés industriels utilisés
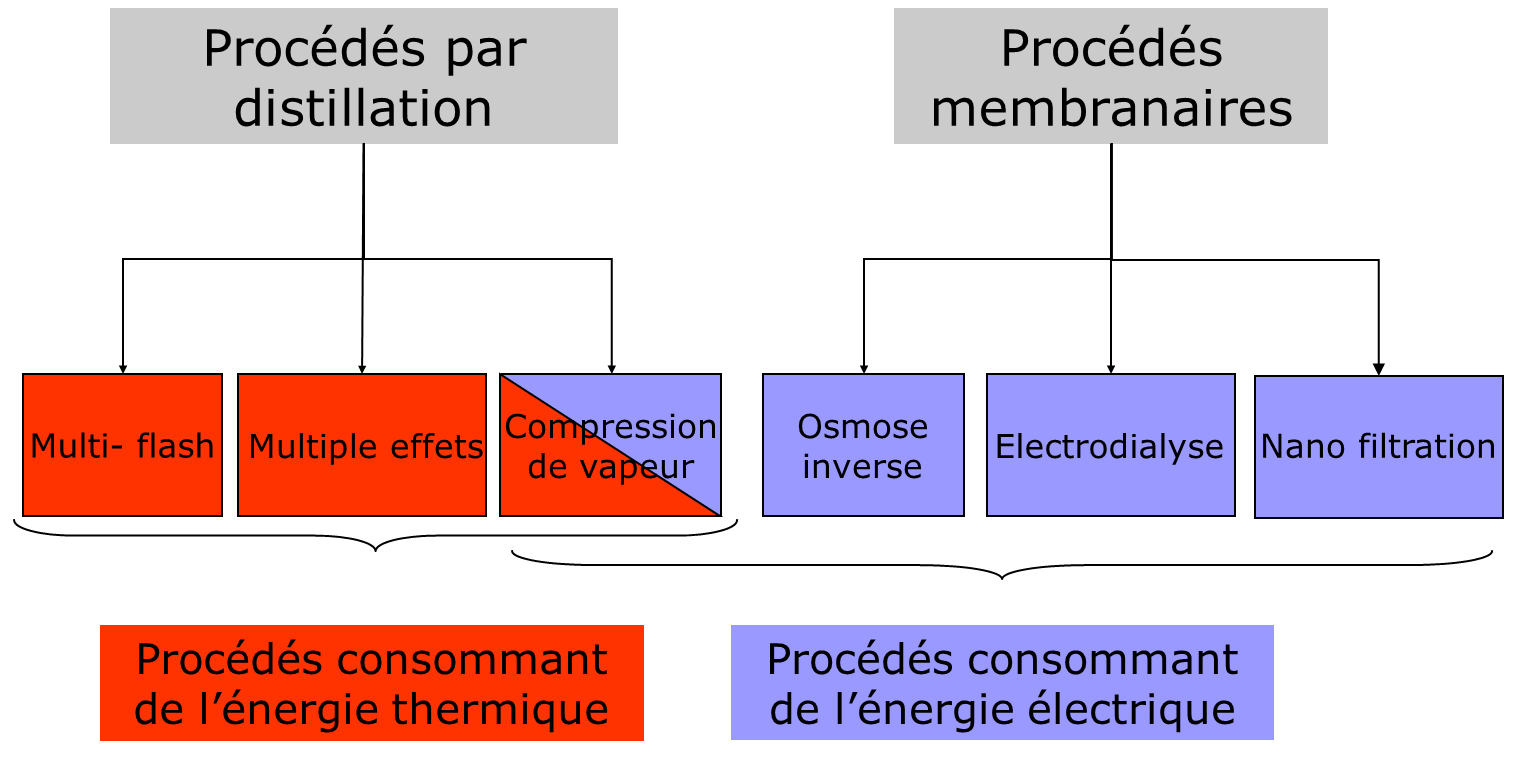
Les principaux procédés industriels actuellement utilisés sont des développements des méthodes présentées précédemment ; ils se classent en deux catégories : les procédés de distillation et les procédés membranaires.
Selon la nature du procédé mis en jeu, la capacité de production peut varier de quelques litres par jour à plusieurs centaines de milliers de mètres cubes par jour. Le choix du procédé mis en œuvre dépend de multiples paramètres mais en premier lieu de la nature de l’eau à traiter – eau de mer ou eau saumâtre, de la capacité de production souhaitée, et de la source d’énergie disponible comme indiqué sur la Figure 6.
À ces deux grandes familles, on peut ajouter des procédés non conventionnels très peu utilisés ou en cours de développement tels que la cristallisation, les cycles à air (humidification-déshumidification d’air), la distillation membranaire, l’osmose directe et bien d’autres encore.
4. L’énergie minimum de dessalement
On comprend bien que la consommation d’énergie est un point clé du dessalement des eaux. On peut alors se poser la question de savoir s’il existe une consommation d’énergie minimum en dessous de laquelle il est impossible de descendre même avec un système idéal, sans perte ni irréversibilité, avec un rendement égal à cent pour cent.
Le minimum d’énergie à dépenser correspond à l’énergie qui compense l’écart ébullioscopique pour la distillation et à l’énergie qui permet de vaincre la pression osmotique pour l’osmose inverse.
Des calculs simples permettent d’avoir une très bonne estimation de cette énergie minimum. Dans le système international, elle s’exprime en Joules par kilogramme d’eau douce produite mais plus communément en kilowattheures par mètre cube d’eau douce (kWh/m3).
Ainsi, pour la distillation, comme l’eau salée bout à une température légèrement supérieure à l’eau pure (Figure 7), si on considère de l’eau de mer et de l’eau pure à la même température de 25°C, il y aura moins de vapeur d’eau au-dessus de l’eau de mer qu’au-dessus de l’eau pure. En d’autres termes, la pression partielle de vapeur d’eau sera plus basse au-dessus de l’eau de mer. Pour obtenir la même pression, il faudrait que l’eau de mer soit légèrement plus chaude que l’eau pure.
Fig. 7 : Courbes Température-Pression de l’eau pure et de l’eau de mer – Source: Philippe Bandelier
L’énergie minimum de dessalement sera donc le travail à fournir pour faire passer un kilogramme de vapeur (m) de la pression qui règne au-dessus de l’eau de mer à celle qui règne au-dessus de l’eau pure. Les tables thermodynamiques[14] nous indiquent ces pressions : 3170 Pa pour l’eau pure, 3105 Pa pour l’eau de mer. La loi de compression isotherme réversible nous donne le travail à fournir WD.
(M, R et T sont la masse molaire de l’eau, la constante des gaz parfaits et la température) :
WD = m/M.R.T.In(Peau douce/Peau de mer)= 0.79kWh/m3
Pour l’osmose inverse, l’énergie minimum à fournir WRO correspond au travail pour transférer un kilogramme d’eau (m) avec un écart de pression égal à la pression osmotique (V et ρeau pure sont le volume transféré et la masse volumique de l’eau) :
WRO = V.Peau de mer osmotique = m/ ρeau douce . Peau de mer osmotique = 0.81kWh/m3
Il est assez remarquable que les deux calculs correspondant à des principes physiques totalement différents conduisent finalement à des résultats aussi proches. Mais comme l’état initial – eau et sel mélangés – et l’état final – eau et sel séparés – sont identiques, le premier principe de la thermodynamique impose que l’énergie à mettre en jeu doit être la même dans les conditions de réversibilité totale, c’est-à-dire sans aucune perte. On remarquera toutefois que cette énergie minimum est très théorique car on suppose dans les calculs précédents que le taux de conversion est nul, c’est-à-dire qu’on est juste autour de l’équilibre.
5. Les procédés industriels de distillation les plus utilisés
Très rapidement, il est apparu que, pour limiter les phénomènes de corrosion et d’encrassement, et diminuer les inconvénients dus à la présence d’air, il faut opérer sous pression réduite, ce qui abaisse la température de distillation (Rochon, 1813[15]). En effet, la vitesse de corrosion augmente avec la température. L’eau de mer contient, en plus du chlorure de sodium, des sulfates et des carbonates de calcium et de magnésium qui sont des sels à solubilité inverse : une température élevée favorise leur précipitation sous forme de tartre. Si un nettoyage chimique permet d’éliminer le tartre formé par les carbonates, les sulfates sont quasiment insolubles. On doit donc choisir des températures de fonctionnement qui évitent leur formation. Sans traitement chimique préventif, la température maximum de l’eau de mer est généralement limitée à une soixantaine de degrés. La pression correspondante est environ 200 hectopascals (1 hPa = 1 millibar, mbar), soit un peu moins d’un cinquième de la pression atmosphérique. On parle de distillation sous pression réduite.
Par ailleurs différents procédés de distillation ont été développés dans le but de réduire l’énergie thermique consommée. La performance thermique des procédés de distillation est caractérisée par le Gain Output Ratio (GOR) qui est un nombre sans unité, généralement le rapport entre le débit d’eau produite, exprimé en tonnes par heure, et le débit de vapeur consommée, également en tonnes par heure.
5.1. Le procédé de vaporisation instantanée (MSF) pour la production massive
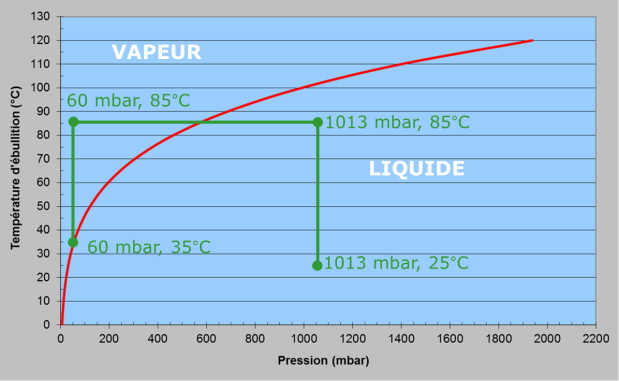
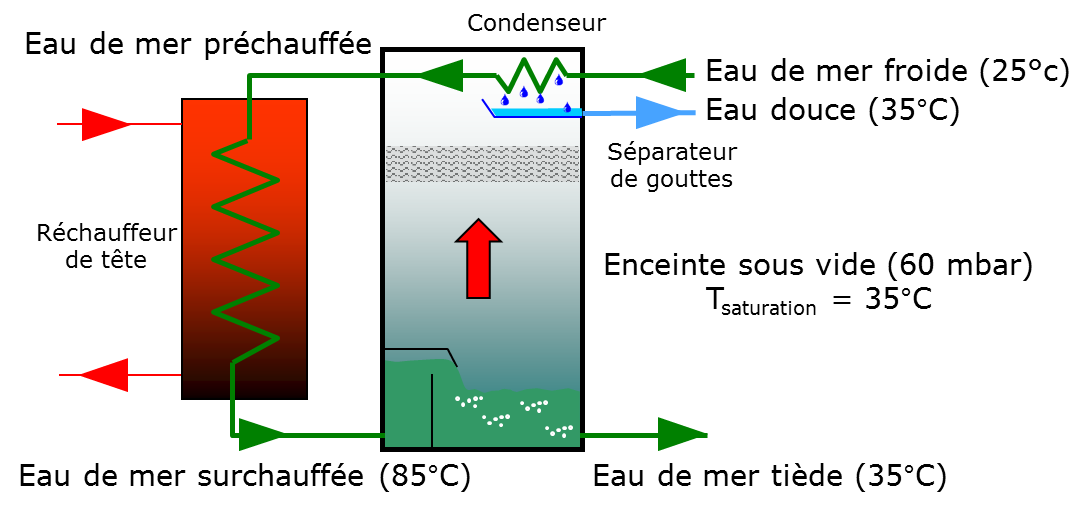
La vaporisation instantanée, plus connue sous son appellation anglo-saxonne MSF pour Multi-Stage Flash, consiste à chauffer l’eau de mer (de 25 °C à 85 °C, à la pression de 1013 mbar, sur la Figure 8) puis à l’introduire dans une suite de cellules où la pression est inférieure à la pression de saturation[16] (passage de 1013 à 60 mbar sur la figure). L’eau surchauffée va donc bouillir spontanément et assez violement – d’où le nom de « flash » – pour retourner à l’état d’équilibre thermodynamique (pression 60 mbar, température 35 °C). La vapeur produite est condensée en utilisant l’eau de mer qui est ainsi préchauffée, ce qui permet d’économiser une partie de l’énergie nécessaire (Figure 9).
Le bilan d’énergie s’écrit :
P.Hν = M.Cp.(Tsurchauffe – Tsaturation)
où P est la quantité d’eau vaporisée, Hv l’enthalpie de vaporisation de l’eau, M le débit d’eau qui « flashe » et Cp la capacité calorifique de l’eau.
On observe que la quantité d’eau ainsi vaporisée (P) est directement proportionnelle à l’écart de température lors de la détente. Pour les valeurs courantes, le débit d’eau qui « flashe » (M) vaut approximativement dix fois le débit d’eau produite.
Si théoriquement un seul étage de détente serait suffisant, pratiquement on observe que l’équilibre thermodynamique n’est pas atteint entre l’eau de mer après détente et la température de saturation dans l’enceinte. Ce déséquilibre est la conséquence des différentes pertes thermodynamiques dont l’écart ébullioscopique et l’écart résiduel de détente. Par ailleurs, opérer la détente en un seul étage limite considérablement la possibilité de récupérer l’énergie thermique au condenseur. Ces deux limites invitent à placer plusieurs étages en série.
Pratiquement, la détente s’effectue donc dans plusieurs cellules jusqu’à 16 voire même plus, dans lesquelles la pression et la température décroissent progressivement. Entre deux étages, la température décroit de seulement trois ou quatre degrés. La récupération de chaleur est alors maximum et les pertes thermodynamiques sont minimisées. En dessous, le déclenchement de la vaporisation devient aléatoire à cause des irréversibilités qui deviennent prépondérantes. Et l’investissement devient tellement important qu’un nombre d’étages très important n’a plus de justification économique.
Du fait de l’absence d’échangeur de chaleur pour l’évaporation, le procédé est moins sujet à l’entartrage que les autres. Néanmoins, le problème est reporté sur le réchauffeur de tête qui fonctionne alors dans des conditions particulières (vitesse de circulation élevée pour limiter les incrustations, traitement tartrifuge).
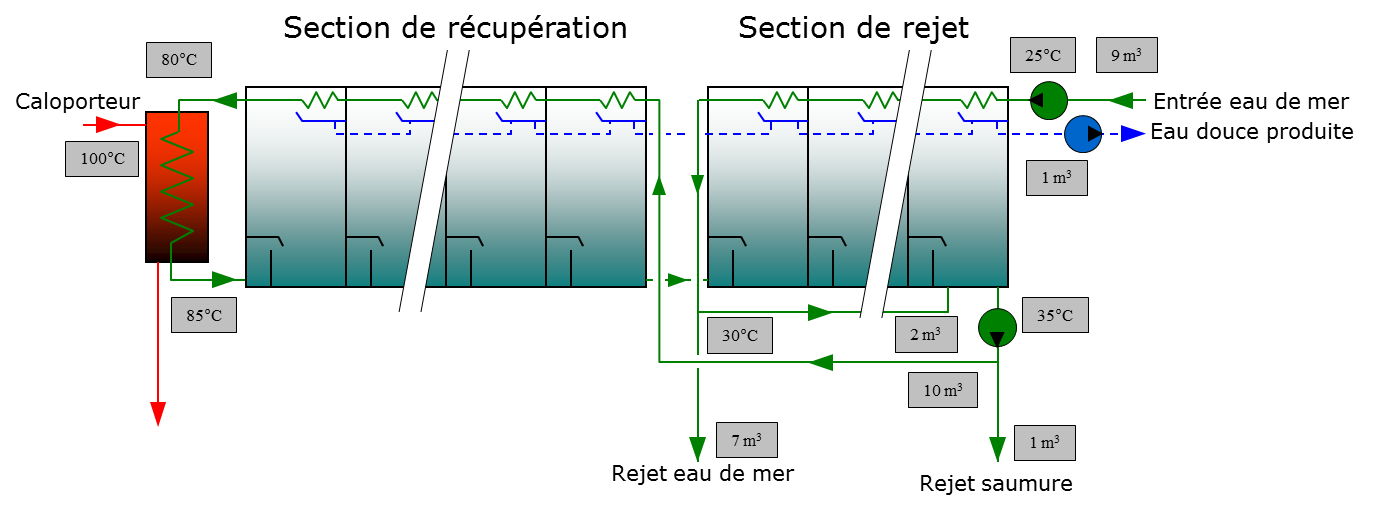
Pour optimiser au mieux le schéma thermique, les étages sont disposés en deux sections distinctes, une section de récupération de chaleur et une section de rejet (Figure 10). Le GOR de ce type d’installation varie communément entre 7 et 12.
5.2. Le procédé à multiple-effet (MED) pour économiser l’énergie
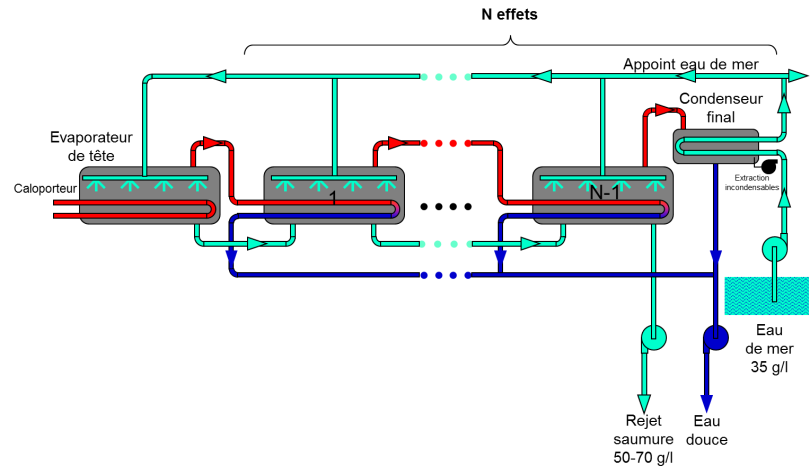
Le procédé à multiple-effet (Multi-Effect Distillation, MED) a été spécifiquement développé dans le but d’économiser l’énergie thermique. Les premières tentatives datent du 19ème siècle. La puissance thermique apportée à l’évaporateur de tête par un fluide caloporteur – fluide qui transporte la chaleur – sert à faire évaporer de l’eau de mer. La vapeur produite est condensée dans l’évaporateur suivant, qu’on appelle le premier effet.
L’enthalpie de condensation sert alors à évaporer à nouveau de l’eau de mer et ainsi de suite jusqu’au condenseur final (Figure 12). Le débit d’eau douce globalement produit est théoriquement égal à la production du premier effet multipliée par le nombre d’effets. D’où le nom de multiple-effet. Les différentes irréversibilités font qu’en réalité on constate une perte de 10 à 20%. Pour que le système puisse fonctionner, il faut bien entendu que les températures et les pressions s’échelonnent de manière décroissante de l’évaporateur de tête vers le condenseur final afin de garantir un écart de température entre la vapeur qui se condense et l’eau de mer qui s’évapore. L’alimentation de chacun des effets en eau de mer peut se faire en parallèle, à co-courant de l’évaporateur de tête vers le dernier effet ou bien à contre-courant bien que cette dernière configuration ne soit pas recommandée puisque les effets les plus chauds en tête se trouvent alors alimentés avec l’eau de mer la plus concentrée, donc dans les conditions les plus encrassantes.
L’énergie thermique consommée décroit d’une manière quasiment linéaire quand le nombre d’effets augmente, ce qui fait que le GOR est égal au nombre d’effets diminué de 10 à 20% à cause des irréversibilités. Les installations à multiple-effet sont maintenant presque toujours combinées avec une compression de vapeur, décrites dans le paragraphe suivant, afin d’augmenter encore les performances énergétiques. Comme pour le procédé « flash », le nombre d’effets est limité à la fois par les irréversibilités qui limitent la réduction de l’écart de température entre les effets à environ deux degrés et aussi par des considérations économiques.
5.3. La compression de vapeur (MVC, TVC) : une façon complémentaire d’économiser l’énergie
La distillation par compression de vapeur est aussi un procédé permettant de produire de l’eau en minimisant la consommation d’énergie. Elle est toujours associée au procédé multiple-effet, le nombre d’effets pouvant être réduit à un seul. Le principe est le même que celui des pompes à chaleur, le fluide de travail subissant le cycle thermodynamique étant cette fois l’eau. Contrairement à une pompe à chaleur, le circuit du fluide thermodynamique est ouvert au lieu d’être fermé. La compression peut être réalisée avec un compresseur mécanique (Mechanical Vapor Compression, MVC) ou avec un thermocompresseur (Thermal Vapor Compression, TVC).
5.3.1. Compression mécanique de vapeur (MVC)
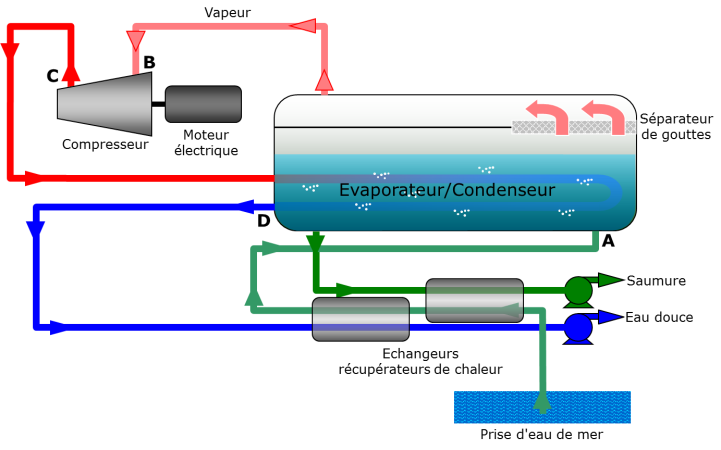
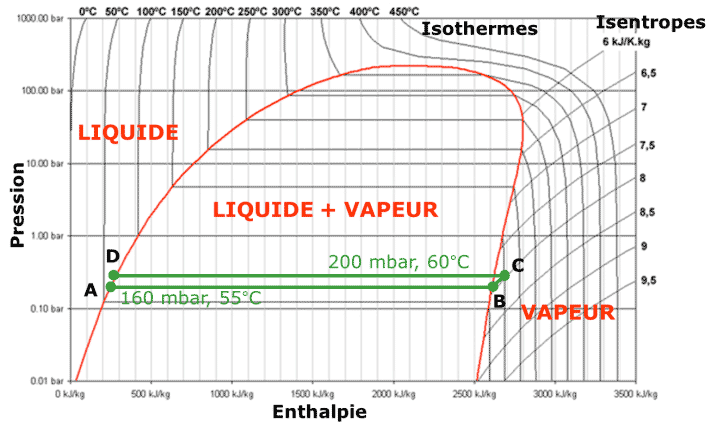
L’eau de mer liquide et préchauffée (point A des Figures 14 et 15 ) est évaporée à 55 degrés sous une pression réduite à 160 millibars (mbar) (A→B). La vapeur obtenue est très légèrement comprimée à 200 mbar (B→C). La température de saturation est alors de 60 degrés. Cette vapeur est ensuite condensée (C→D) mais la chaleur latente de condensation à 60 degrés est utilisée dans l’évaporateur/condenseur pour évaporer l’eau de mer à 55 degrés. L’eau pure, liquide (D), peut alors être extraite ainsi que la saumure correspondant à la fraction d’eau de mer non évaporée. Comme ces deux fluides sont extraits à 55 et à 60 degrés, ils sont utilisés pour préchauffer l’eau de mer introduite dans le système. En dehors du réchauffage initial néessaire pour démarrer l’installation, la principale consommation d’énergie est l’énergie électrique du compresseur. Celle-ci est minimisée du fait que l’écart de température est faible. Le taux de compression correspondant est donc aussi très faible. Là encore, la limite est économique car plus l’écart de température est petit (mais toujours limité par les irréversibilités) plus la surface d’échange nécessaire pour évaporer et condenser sera grande.
5.3.2. Thermocompression de vapeur
La taille des usines de dessalement n’ayant jamais cessé de croitre, la compression mécanique a rapidement été inadaptée aux grosses installations, à cause des limites à la fois techniques et économiques pour le compresseur. Même si le rendement diminue très vite quand le taux de compression augmente, la thermocompression s’est rapidement imposée car l’investissement et le coût de maintenance sont extrêmement bas.
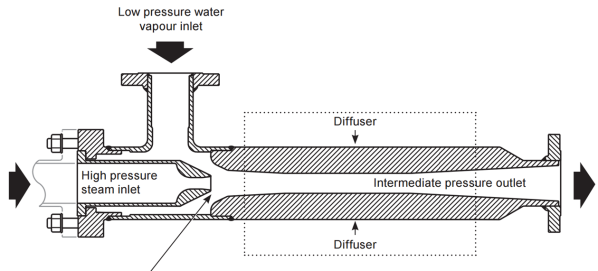
Le principe est d’utiliser une tuyère dans laquelle, par accélération dans un injecteur et un col, de la vapeur haute pression aspire de la vapeur basse pression pour obtenir de la vapeur à pression moyenne. La compression s’opère entre la vapeur à basse pression aspirée et le mélange à pression moyenne qui est restitué. La seule source d’énergie étant la vapeur haute pression, c’est bien un procédé « thermique » de compression. Les performances sont caractérisées par le débit de vapeur motrice à haute pression nécessaire pour entrainer la vapeur à basse pression (consommation de vapeur par unité de vapeur aspirée) ou bien par le taux d’entrainement (débit entrainé par unité de vapeur motrice).
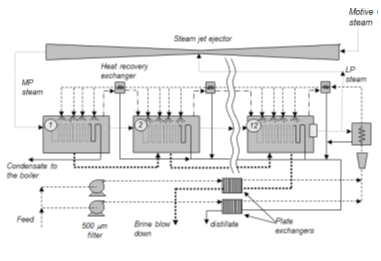
La thermocompression est toujours combinée avec le procédé à multiple-effet (Figure 18). La recompression de la vapeur peut s’effectuer entre le dernier et le premier effet ; dans ce cas le taux de compression est maximum et le rendement de compression peu élevé, ce qui se traduit par une consommation de vapeur haute pression élevée. Mais elle peut aussi se faire entre un étage intermédiaire et le premier effet, le rendement est alors bien meilleur et la consommation de vapeur plus basse.
5.4. Comparaison des différents procédés de distillation
Les données issues des travaux de Mahmoud Abdel-Jawad (2001)[17] et Wangnick (2004)[18] permettent une comparaison des différents procédés de distillation. Une synthèse est donnée dans le Tableau 1.
Tableau 1 : Caractéristiques des différents procédés de distillation
| MSF | MED | MVC | MED-TVC | |
| Température de tête °C | <120 | <70 | <70 | <70 |
| Source d’énergie principale | Vapeur | Vapeur, eau chaude | Electricité | Vapeur |
| Consommation thermique kWh/m3 | 70 – 80 | 50 – 70 | 0 | 50 – 60 |
| Consommation électrique kWh/m3 | 3.5 | 1.5 | 8 -14 | 1.5 |
| Capacité par ligne m3/j | 5 000 – 70 000 | 500 – 12 000 | 10 – 2 500 |
100 – 25 000 |
La distillation a été pendant longtemps le procédé exclusif de dessalement. Mais avec le renchérissement de l’énergie thermique, le marché s’est progressivement tourné vers les procédés membranaires. Si aujourd’hui environ la moitié de l’eau douce issue de l’eau de mer est produite par distillation, c’est grâce aux très grosses usines de dessalement du Moyen-Orient couplées à des centrales électriques qui les alimentent en énergie thermique à faible coût marginal. La situation pourrait radicalement changer lorsque ces usines arriveront en fin de vie.
6. L’essor des procédés membranaires dominé par l’osmose inverse
Longtemps réservé au dessalement des eaux saumâtres et aux petites capacités, l’osmose inverse, procédé mis au point au cours du vingtième siècle, a bénéficié des progrès réalisés sur les membranes et sur les systèmes de récupération d’énergie qui ont littéralement fait exploser son marché. Aujourd’hui, si on considère l’ensemble des eaux traitées, l’osmose inverse représente presque les deux tiers de la capacité installée. Il écrase les autres procédés membranaires qui sont essentiellement l’électrodialyse, la distillation membranaire et l’osmose directe.
D’autres procédés qui seront énumérés plus loin utilisent aussi des membranes mais leur développement n’est pas encore très avancé.
6.1. L’osmose inverse (RO)
6.1.1. Des membranes aux qualités exceptionnelles
Le principe de l’osmose inverse (Reverse Osmosis, RO) est de disposer d’une membrane séparatrice poreuse dont la taille des pores est suffisamment petite – quelques nanomètres – pour laisser passer les molécules d’eau mais pas les ions, beaucoup plus gros. Malheureusement, la séparation n’est pas parfaite et un peu de sel traverse quand même la membrane. Des traitements de fonctionnalisation peuvent renforcer le caractère sélectif de ces membranes et accroitre leur capacité de séparation.
Pour limiter les pertes de charge dues à l’écoulement de l’eau à travers ces membranes et donc minimiser la consommation d’énergie, elles sont extrêmement fines : leur épaisseur est souvent une fraction de micron. La pression osmotique s’opposant à l’écoulement dès que de l’eau pure traverse la membrane, il faut appliquer sur l’eau à traiter une pression au moins égale à la pression osmotique afin de forcer le flux dans le sens de la séparation. La membrane ne fonctionne donc pas complètement à la manière d’un filtre car l’écoulement doit vaincre la pression osmotique en plus. On a vu que cette pression vaut 29 105 Pa pour l’eau de mer ; elle augmente au fur et à mesure du processus de concentration. Pratiquement, pour concentrer et obtenir un flux significatif, la pression de fonctionnement est de l’ordre de 60 à 70 105 Pa et le taux de conversion de l’eau de mer en eau douce est légèrement inférieur à 50%. Bien sûr, si l’eau est faiblement salée, la pression à appliquer diminue et le taux de conversion peut être augmenté, ce qui a conduit à imposer l’osmose inverse comme le procédé de référence du traitement des eaux saumâtres.
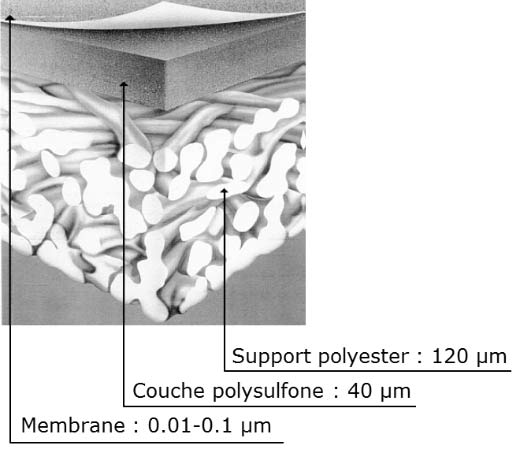
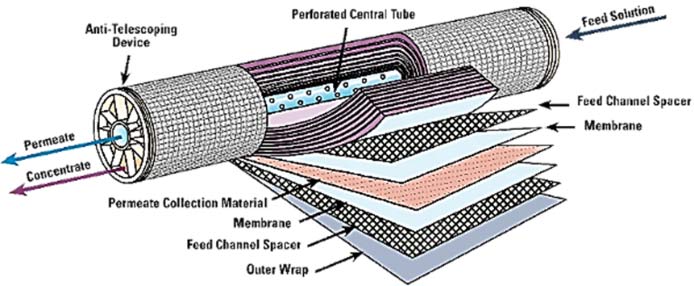
Travailler à haute pression induit une seconde conséquence. Les membranes doivent résister à des écarts de pressions très importants. Il existe différents types de membranes : à fibres creuses ou en film. Les fibres creuses sont des capillaires dont le diamètre intérieur mesure typiquement quelques dizaines de microns tandis que le diamètre extérieur est de dimension millimétrique. Grâce à ces petites dimensions, leur résistance à la pression est excellente. Mais bien que leur surface par unité de volume soit très supérieure à celle des films – dans un rapport de 10 :1 – elles sont très peu utilisées pour des questions d’encrassement et de bouchage. Pour les membranes en film, la couche active extrêmement mince ne résiste pas seule à la pression. Elle est donc associée à d’autres couches très poreuses qui lui servent de support et lui assurent des propriétés mécaniques adéquates (Figure 19).
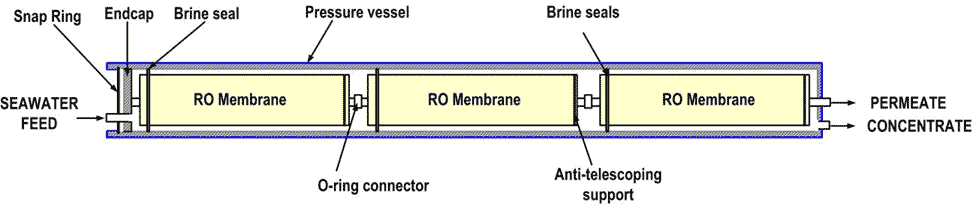
Les films ainsi constitués sont enroulés avec des espaceurs qui forment des canaux pour l’eau salée et pour l’eau pure (Figure 20). Un module ainsi constitué développe une surface de l’ordre de 40 m² pour un diamètre de 200 millimètres (8 pouces) et une longueur de 1 mètre (40 pouces). Plusieurs modules, typiquement sept, sont ensuite assemblés dans un tube de pression (Figure 21) ; des dizaines de tubes assemblés en parallèles constituent un train.
Les tubes de pression sont ensuite associés en très grand nombre – plusieurs dizaines – d’une manière modulaire, chaque module s’appelant un train, ce qui permet d’atteindre des productions très importantes comme à Ashkelon (Figure 22).
6.1.2. Un souci d’économie d’énergie
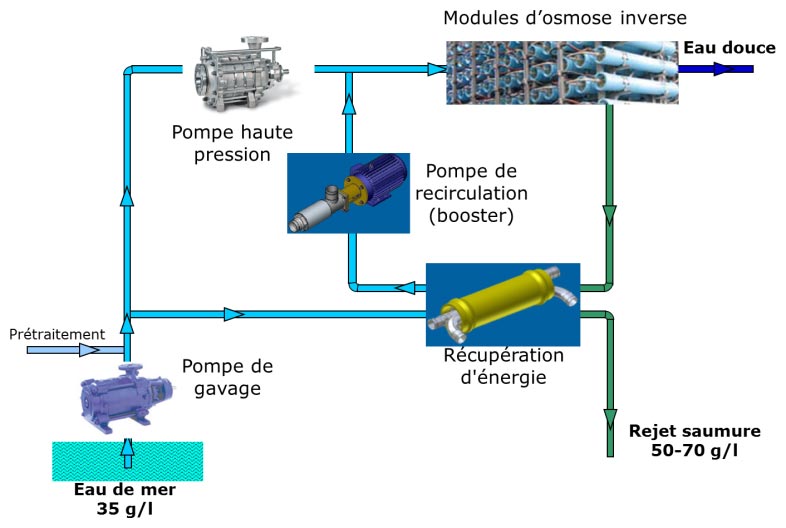
Comme pour les procédés de distillation, la consommation énergétique de l’osmose inverse est une préoccupation majeure. Puisque seulement la moitié de l’eau est extraite sous forme d’eau douce à partir de l’eau salée, l’unité rejette une saumure concentrée à une pression très élevée, de l’ordre de 60-70 105 Pa, quasiment égale à la pression de fonctionnement de l’osmoseur. Très rapidement, des dispositifs récupérant cette énergie de pression ont été intégrés (Figure 23). Des turbines ou des systèmes analogues ont été introduits au début des années 80. La saumure haute pression est dirigée sur une turbine disposée sur le même axe que la pompe haute pression de l’osmoseur, celle-ci consomme alors 30 à 40% de puissance en moins. Ensuite, et bien que décrits dès les années 50, l’emploi d’échangeurs de pression – systèmes isobariques – s’est généralisé à partir des années 2000.
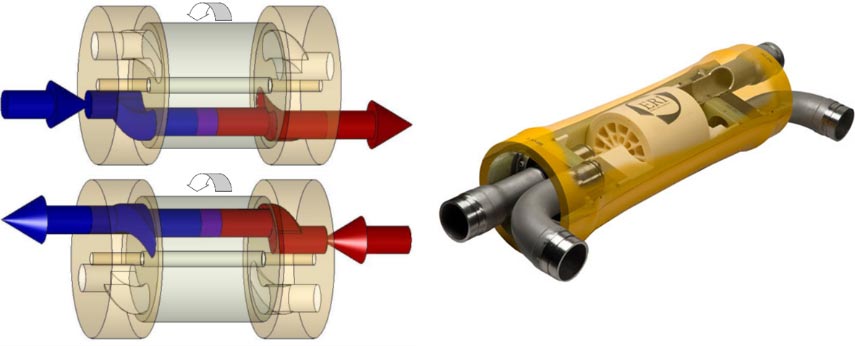
Le principe de l’échangeur de pression est basé sur un canal cylindrique dans lequel la saumure sous pression chasse l’eau de mer vers l’osmoseur alternativement avec l’eau de mer qui chasse la saumure vers le rejet. Un ensemble de clapets et de tiroirs assure la distribution alternative des fluides et un piston sépare les fluides. Deux cylindres fonctionnent en tandem pour assurer une continuité de tous les débits. Mais le système le plus élaboré est l’échangeur de pression développé par la société ERI[19] (Figure 24) car il est rotatif et ne comporte ni clapet ni piston. C’est la pression de la saumure qui assure la rotation du dispositif à une vitesse de 1200 tours par minute. Le rendement de récupération est supérieur à 95%. A cause de l’absence de piston, les fluides se mélangent partiellement mais seulement de quelques pour cent.
En première approximation, les transferts dans un module d’osmose inverse peuvent être décrits par des relations simples :
Flux d’eau à travers la membrane : J1=A.(ΔP – Δπ)
Flux de sel à travers la membrane : J2=B.(C0 – Cp)
Taux de rejet du sel : TR=A.(ΔP–Δπ))/(A.(ΔP–Δπ )+B)
Où J1 et J2 sont exprimés en kg/m².s
A est la perméabilité de la membrane (3 10-9 kg/m².s.Pa, 1 l/m².h.bar)
B la perméabilité au sel (10-7 m/s)
ΔP l’écart de pression moyen Pa
Δπ l’écart de pression osmotique moyen Pa
C0 – Cp l’écart de concentration kg/m3
La consommation d’énergie de la pompe haute pression résulte d’un compromis entre la pression de fonctionnement, le taux de conversion et la surface de membranes installée. Typiquement, pour le dessalement d’eau de mer, la pression de fonctionnement est fixée entre 60 et 70 105 Pa, le taux de conversion est un peu inférieur à 50% et la surface de membrane est environ 2 m²/(m3/j). La consommation d’énergie est comprise entre 3 et 4,5 kWh/m3. Pour dessaler de l’eau saumâtre dont la concentration en sel est cinq grammes par litre, la pression optimale est divisée par deux, le taux de conversion atteint 70% mais la surface de membrane reste sensiblement identique. La consommation d’énergie descend entre 1,5 et 2 kWh/m3.
6.1.3. Encrassement – Prétraitement
Bien que l’osmose inverse ne soit pas du tout un procédé thermique, les membranes sont sujettes à l’encrassement qui se manifeste par des dépôts aussi bien minéraux du type tartre, qu’organiques (encrassement biologique). Outre l’aspect sanitaire, ces dépôts altèrent les performances de transfert des membranes, qui par ailleurs vieillissent, ce qui conduit à les remplacer périodiquement. Toutefois, entre deux changements, des traitements chimiques permettent de maintenir ou de rétablir un état assurant des performances acceptables. Ces traitements sont regroupés dans ce qu’on appelle le prétraitement de l’eau de mer, avant de procéder à l’osmose inverse. Ce poste représente environ 10% de l’investissement total et 10% du prix final de l’eau. Il nécessite une surveillance très stricte au risque de détruire irrémédiablement les membranes. Sans être systématiquement toutes obligatoires, les différentes étapes du prétraitement sont :
- Une filtration sur différents types de filtres, dont la micro et l’ultrafiltration
- Une floculation, elle améliore la qualité de la filtration ; on utilise des sels ferriques ou des polyélectrolytes pour agglomérer les particules en suspension et les décanter
- Un traitement antitartre, à base d’acides ou de phosphates
- Un traitement inhibiteur de corrosion à base de polyphosphates
- Une désinfection au chlore ou à l’hypochlorite de sodium pour éliminer les micro-organismes présents dans l’eau
- Une neutralisation du désinfectant aux sulfites car, à base de chlore ou de dérivé chloré, le désinfectant attaque les membranes
- Un ajustement du pH car les propriétés de transfert des membranes y sont sensibles
- Un contrôle de la température
Des travaux ont été menés pour déterminer la température de fonctionnement optimale d’un osmoseur. En effet, par diminution de la viscosité de l’eau, une élévation de température augmente la production de 2 à 3% par degré. Malheureusement, la salinité de l’eau produite augmente aussi de 2% par degré et la durée de vie des membranes est abrégée. Finalement, pour assurer une durée de vie de l’ordre de deux à quatre ans, on constate que la température doit être comprise dans une fourchette très réduite de quelques degrés autour de 28 degrés. La température est donc un paramètre qui est surveillé et non pas un paramètre de fonctionnement ajustable, tout au moins dans les pays chauds.
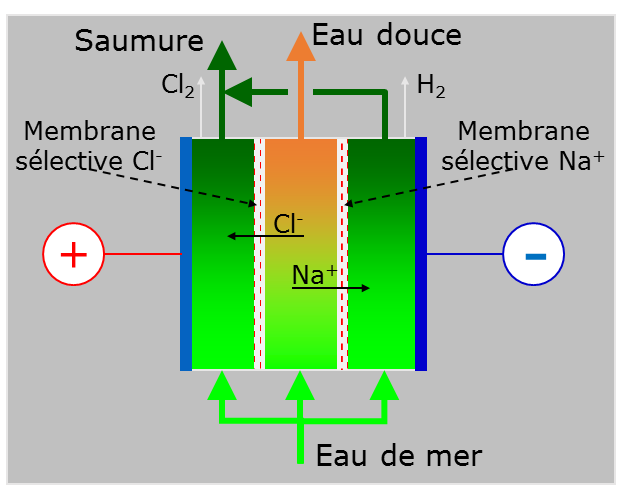
6.2. L’électrodialyse (ED) pour extraire le sel des eaux saumâtres
L’électrodialyse (Électrodialyses, ED) a été développée dans les années 60. Le principe n’est pas d’extraire l’eau pure de l’eau à traiter mais au contraire d’en extraire les ions chlorure et sodium à travers des membranes sélectives. La migration des ions est provoquée par un champ électrique (Figure 25). Si ce procédé est bien adapté au traitement des eaux saumâtres, peu concentrées, la consommation électrique devient rédhibitoire au-delà d’une salinité de 4 grammes par litre. Pour une tension de fonctionnement de 500 V aux bornes d’un empilement de membranes, la consommation électrique est de 2,6 kWh/m3 pour une concentration initiale de 2,5 grammes par litre, 3,9 kWh/m3 pour 3,5 grammes par litre et 5,5 kWh/m3 pour cinq grammes par litre[20]. À des concentrations aussi basses, l’osmose inverse est donc rapidement plus pertinente sur le plan énergétique.
On notera que le procédé est parfaitement réversible, c’est-à-dire qu’il permet de produire de l’électricité à partir d’eau salée et d’eau douce. Dans la mesure où la production électrique maximum peut se calculer aisément à partir de la formule donnant l’énergie minimum de dessalement, on comprend aisément que le procédé ne présente un quelconque intérêt que si l’eau salée est très concentrée, proche de la saturation. Des expériences ont été menées en utilisant de l’eau saturée de marais salant et, non pas de l’eau douce trop précieuse, mais de l’eau de mer. L’intérêt reste néanmoins anecdotique car, à la faible production d’électricité, il faut retrancher la puissance électrique consommée par les pompes de transfert.
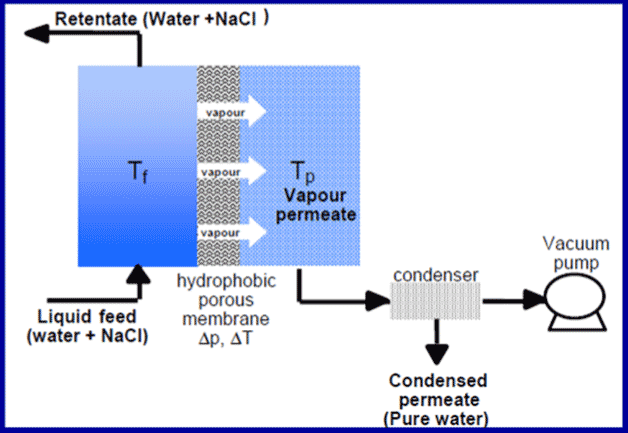
6.3. La distillation membranaire (MD), un procédé intéressant encore en développement
Proche de l’osmose inverse en ce sens qu’on extrait l’eau, la distillation membranaire (Membrane Distillation, MD), procédé qui date des années 60, en diffère par le fait qu’on utilise un écart de pression de vapeur comme force motrice, et non pas la pression au sens mécanique, pour réaliser le transfert (Figure 27)[21]. C’est donc un procédé membranaire atypique qui consomme principalement de l’énergie thermique.
La distillation membranaire ne doit pas être confondue avec la pervaporation qui combine en plus des phénomènes d’adsorption et de désorption. Les membranes sont hydrophobes et fonctionnent exactement de la même manière que les textiles techniques recouverts d’une membrane hydrophobe fluorée qui constitue une barrière à la pluie mais évacue la vapeur d’eau de la transpiration. Le procédé fonctionne autour de 70 degrés à l’entrée côté chaud, l’écart de température avec le côté froid est de 10 à 20 degrés. Sous l’effet de cet écart de température induisant un écart de pression partielle de vapeur d’eau, de la vapeur migre à travers la membrane et se condense au point froid (Figure 26). Le système fonctionne en dépression afin qu’il n’y ait aucun air résiduel qui pénaliserait les transferts par diffusion. Afin de réduire la consommation d’énergie, l’eau salée qui parcourt le condenseur se réchauffe et c’est donc préchauffée qu’elle pénètre dans le réchauffeur de tête. Ce schéma thermique est tout à fait comparable à celui du procédé MSF.
Les membranes ont une épaisseur de 40 à 250 micromètres (µm) et sont réalisées en polyfluorure de vinylidène (PVDF), en polypropylène (PP) ou en polytetrafluoroéthylène (PTFE, bien connu sous le nom de Teflon™). La taille des pores ne dépasse pas 0,2 micromètres. L’intérêt est de pouvoir réaliser une distillation dans un dispositif très compact en utilisant une source de chaleur à basse température avec une consommation électrique des pompes annexes très basse – de l’ordre du kilowattheure par mètre cube d’eau produite. Comparées à l’osmose inverse, les membranes ont une très bonne sélectivité et sont surtout beaucoup moins sensibles à l’encrassement et aux oxydants utilisés comme biocide. Le prétraitement est donc très simplifié. Néanmoins, le stade industriel n’a jamais été atteint pour le dessalement à cause des faibles flux de vapeur obtenus à travers les membranes et finalement de la consommation d’énergie thermique qui reste élevée pour maintenir un flux significatif. Le GOR ne dépasse pas 4 à 6. Les prototypes réalisés montrent la compacité des installations (Figure 28)[22].
7. Beaucoup de procédés possibles de dessalement des eaux en cours de développement
Partant du constat que les procédés courants consomment beaucoup plus d’énergie que l’énergie minimum de dessalement, même si celle-ci ne pourra jamais être atteinte, beaucoup d’investigations ont été menées pour imaginer des procédés de dessalement qui soient économes en énergie, simples et globalement le moins coûteux possible pour accroitre l’accessibilité à l’eau des populations. Si beaucoup de travaux sont actuellement en cours, les principes de base avaient souvent été établis dès les années 60, voire même avant. Les progrès récents réalisés dans les nanotechnologies et plus particulièrement dans les nanomatériaux ont ouvert de nouvelles perspectives. Les biotechnologies semblent également offrir des possibilités. Voici quelques technologies de dessalement non conventionnelles, dont certaines n’ont pas connu de développement alors que d’autres sont considérées comme prometteuses.
La congélation est un procédé naturel. La glace d’eau de mer formant la banquise est beaucoup moins salée que la mer. L’eau étant très majoritaire dans le mélange eau + sel, de la glace d’eau douce se forme en premier lors de la congélation. Malheureusement, de petites poches d’eau de mer sont emprisonnées dans la glace et polluent l’eau douce obtenue ensuite en fondant la glace. Le procédé est malgré tout séduisant car l’enthalpie de solidification de l’eau est très inférieure à celle de vaporisation : 335 kJ/kg (93 kWh/m3) contre 2260 kJ/kg (630 kWh/m3). Il faut néanmoins noter que le froid nécessaire à la congélation doit être produit par une machine frigorifique qui consomme une énergie noble, électrique (groupe frigorifique) ou thermique à température moyenne (machine à absorption). Quoi qu’il en soit, même ramené à une source d’énergie primaire, le bilan énergétique reste très en faveur de la congélation. Le froid, stocké sous forme de glace, peut être utilisé pour des usages de climatisation de locaux. Quelques installations pilotes ont été réalisées dans les années 60 aux États-Unis, en Israël et au Royaume-Uni mais vu les performances finalement médiocres et les problèmes de pureté de l’eau produite, il n’y a pas eu de suite.
L’osmose directe (Forward Osmosis, FO) semble se développer. Le principe de cette technique membranaire est de mettre l’eau de mer au contact d’une solution très concentrée, à travers une membrane qui ne laisse passer que l’eau. Sous l’effet du très fort gradient de concentration, l’eau va migrer vers la solution concentrée. Celle-ci est une solution d’un sel volatil, comme par exemple du carbonate d’ammonium. La solution diluée obtenue va donc être chauffée afin de chasser le sel volatil sous forme d’ammoniac gazeux et de gaz carbonique. Ces deux gaz sont à nouveau dissous dans une partie de l’eau épurée obtenue pour reconstituer la solution concentrée tandis que l’autre fraction subit une finition (osmose inverse ou nanofiltration) pour éliminer les traces résiduelles de carbonate d’ammonium. L’ensemble du procédé ne nécessite qu’un peu de chaleur à une cinquantaine de degrés pour régénérer la solution et un peu d’électricité pour les pompes de circulation. La comparaison avec l’osmose inverse semble en faveur de l’osmose directe pour les forts taux de conversion[23].
L’idée d’utiliser une extraction par solvant pour le dessalement n’est pas nouvelle[24]. Deux stratégies sont possibles : soit on extrait l’eau vers le solvant, soit on extrait le sel. Dans tous les cas le solvant doit être régénéré par chauffage et recyclé ; il faut donc que son pouvoir solvant varie beaucoup avec la température. Toute la pertinence du procédé réside donc dans le choix du solvant. Pour extraire l’eau, les amines secondaires et tertiaires sont utilisables bien que leur concentration résiduelle dans l’eau produite rende indispensable une purification finale. Pour extraire le sel, ce qui est beaucoup plus rare car l’eau et le solvant doivent être totalement immiscibles, des solvants polymériques sont utilisables. Vus les enjeux potentiels, leur composition est tenue secrète. Cette technique n’est pas encore au stade industriel pour le dessalement.
L’humidification-déshumidification d’air s’est beaucoup développée ces dix dernières années. Il s’agit d’imiter le cycle naturel de l’eau dans la nature. On sature de l’air en humidité par contact avec de l’eau de mer chaude puis l’air chaud et humide obtenu est refroidi afin de condenser l’humidité qu’il contient. L’eau de mer peut être chauffée à partir de n’importe quelle source de chaleur mais une source solaire est souvent privilégiée. La source froide qui permet la condensation est simplement l’eau de mer qui alimente un condenseur. L’avantage de ce procédé est qu’il fonctionne à la pression atmosphérique et que sa simplicité et sa température de fonctionnement permettent d’utiliser massivement des matériaux plastiques peu coûteux. Bien que modestes, les performances sont intéressantes (GOR 4 à 5). Ce procédé est bien adapté aux petites capacités. Les constructeurs[25]se limitent à une capacité d’une cinquantaine de mètres cubes par jour.
La déionisation capacitive consiste simplement à faire passer l’eau à dessaler dans un canal dont les parois sont constituées d’électrodes poreuses. Sous l’effet d’un champ électrique, les ions migrent vers les électrodes dans lesquelles ils restent piégés. Si le canal est suffisamment long – la longueur peut atteindre 10 mètres – l’eau ressort exempte de sel. Périodiquement, la polarité des électrodes est inversée pour chasser le sel ; une saumure concentrée sort alors du canal. Il s’agit là d’un procédé dans lequel on retire bien le sel et non pas l’eau. Il semble fonctionner avec des solutions très chargées – jusqu’à 100 grammes par litre – avec un taux de conversion supérieur à 80% [26].
L’électrodéionisation est un procédé hybride entre l’électrodialyse et le traitement par résines échangeuses d’ions. Elle convient aussi seulement aux eaux faiblement chargées et de faible dureté (< 1 milligramme par litre). Elle permet d’obtenir de l’eau ultra-pure (polissage d’eau osmosée par exemple). Sous l’effet d’un champ électrique, les ions sodium et les ions chlorures sont chassés à travers des membranes sélectives. L’électro-neutralité est rétablie par les ions hydronium et hydroxyle des résines. La dissociation de l’eau sous l’effet du courant électrique permet de régénérer les résines in-situ. Le procédé fonctionne donc en continu sans consommer de produits chimiques[27]
Le procédé Thermo-Ionic[28] est aussi un procédé utilisant des membranes sélectives. De l’eau de mer est concentrée par évaporation par simple pulvérisation dans l’air jusqu’à environ 180 grammes par litre. Elle est ensuite mise au contact d’eau de mer non concentrée à travers une membrane hydrophobe laissant passer les ions sodium d’une part et d’une membrane hydrophobe laissant passer les ions chlorure d’autre part. Sous l’effet du gradient de concentration, les ions migrent de l’eau concentrée vers l’eau de mer non concentrée. Celle-ci est également au contact d’un second circuit d’eau de mer non concentrée à travers des membranes identiques. Ce sont alors les ions de ce second circuit qui vont migrer pour rétablir l’électro-neutralité du premier circuit. Le second circuit s’appauvrit en sel tandis que le premier s’enrichit. Il y a bien dessalement de l’eau en combinant l’effet d’un gradient de concentration puis d’un gradient électrique. Bien que la consommation spécifique soit donnée autour de 1 kilowattheure par mètre cube d’eau douce produite pour faire circuler les fluides, ce qui est très faible, il ne semble pas y avoir d’industrialisation du procédé ; probablement à cause du faible taux de rejet du sel dû aux gradients inverses, défavorables au transfert souhaité.
Étudiée par le Massachusetts Institute of Technology, la concentration ionique par polarisation dérive des nanotechnologies. Un mini canal, d’une taille caractéristique de 500 micromètres, se sépare en deux sous canaux. De l’eau salée alimente le canal principal tandis d’une polarisation électrique est appliquée au niveau de la séparation. Il se produit alors une déplétion locale des ions qui conduit à enrichir le flux qui sort par une branche tandis que l’autre s’appauvrit. Le taux de rejet du sel a été mesuré à 99% pour un taux de conversion de 50%. La consommation spécifique électrique est de 3,5 kilowattheures par mètre cube. Ces performances placent le dispositif à un niveau équivalent à l’osmose inverse. Mais il est évident qu’il est très sensible à l’encrassement et qu’un débit de production significatif – seulement 1 microlitre par minute par dispositif – ne peut être atteint qu’avec un très grand nombre de dispositifs fonctionnant en parallèle. Une architecture permettant de passer à un débit mille fois supérieur a été testée mais on est encore loin d’un procédé industriel[29].
Les hydrogels sont des polymères hydrophiles qui ont la propriété d’absorber l’eau contenue dans l’eau salée dans laquelle ils sont plongés. Après rinçage, ils peuvent restituer l’eau qu’ils ont absorbée soit par chauffage soit par pressage. Toute autre stimulation est envisageable pour restituer l’eau : pH, champ électrique ou magnétique, lumière, etc. Leur base est un polyacrylate fonctionnalisé pour lui conférer les bonnes propriétés. La capacité d’absorption est de l’ordre de 1000 fois en masse. Le temps caractéristique d’un cycle est d’une trentaine de minutes. L’énergie à mettre en jeu pour récupérer l’eau semble être un point actuellement très limitant : entre 20 et 40 kilowattheure par mètre cube par pressage mécanique[30].
Les hydrates de gaz (chlathreates) sont des cristaux se présentant comme de la glace mais ils sont formés de molécules d’eau qui piègent un gaz tel que du méthane ou du dioxyde de carbone. Beaucoup d’autres gaz peuvent être envisagés. La proportion d’eau piégée est 85% dans le cas du méthane. Une fois formés, il suffit de séparer les hydrates, solides, de la saumure et de les décomposer pour obtenir de l’eau et recycler le gaz. Le principe avait été identifié dès les années 40 sans y prêter plus d’attention à l’époque. Malheureusement la présence de sel à tendance à inhiber la formation des hydrates. La formation d’hydrates a lieu typiquement autour de zéro degré sous plusieurs bars de pression pour le cas d’hydrate de propane. Le fait qu’il faille refroidir l’eau de mer et le gaz pour former l’hydrate sous pression puis chauffer pour le décomposer rend encore le procédé très discutable pour une utilisation industrielle. Néanmoins, le champ est totalement ouvert pour trouver un couple eau/gaz plus performant[31].
Le biodessalement est basé sur l’affinité de certaines plantes ou de bactéries pour le sel. Des expériences ont été menées avec des cyanobactéries et avec une variété de nénuphar. La lumière solaire est la source d’énergie permettant les transferts. La séparation n’est pas totale, pour l’instant seules des variations de concentration ont été observées. Le sel extrait se retrouve incorporé à la biomasse produite[32].
Les procédés de captation d’humidité fournissent une alternative intéressante pour les petites capacités. Comme la nature procède naturellement à la première étape de la distillation en évaporant l’eau de mer, de la vapeur d’eau est finalement présente partout dans l’atmosphère, il ne reste plus qu’à la condenser pour obtenir de l’eau douce. Si le site s’y prête, comme par exemple sur les iles océaniques, la condensation sous forme de brouillard se produit aussi naturellement durant la nuit. De l’eau peut alors être collectée par des toiles tendues sur lesquelles les gouttelettes du brouillard s’impactent, coalescent et ruissellent. Avec une humidité relative de 100%, on peut ainsi récupérer jusqu’à 2 litres d’eau par nuit et par mètre carré de toile[33].
Pour « forcer » la formation de rosée, des surfaces émissives peuvent abaisser la température de capteurs d’humidité sur lesquels l’humidité ambiante va se condenser. Ces systèmes fonctionnent aussi la nuit, quand l’humidité relative est maximum et que le rayonnement du capteur vers le ciel nocturne permet le refroidissement. Enfin, on peut aussi utiliser une machine frigorifique pour abaisser la température de l’air sous son point de rosée et obtenir ainsi de l’eau par condensation[34]. Ce dernier principe reste très énergivore car il nécessite de refroidir beaucoup d’air pour obtenir peu d’eau (130 mètre cube d’air par litre d’eau pour un climat à 30 degrés et 40% d’humidité relative).
Des pièges à humidité sont également étudiés. Ils sont constitués d’un tapis de nanotubes de carbone dont l’extrémité exposée à l’air est hydrophile tandis que celle au bas des tubes est hydrophobe. L’ensemble présente un caractère hygroscopique, c’est-à-dire qu’il capte spontanément l’humidité environnante et l’eau se piège dans l’assemblage. Une masse d’eau égale à 80% de la masse des nanotubes a été obtenue en 13 heures dans de l’air saturé. L’évaporation semble très ralentie une fois l’eau piégée. La récupération de l’eau nécessite un pressage[35].
L’ensemencement de nuages pour provoquer artificiellement la pluie a été expérimenté. On peut utiliser des ions obtenus par ionisation de l’air comme germes, des cristaux d’iodure d’argent ou simplement des cristaux de glace.
8. Considérations environnementales
Le dessalement est-il écologique ? C’est un vaste débat. Si une enquête réalisée au début des années 2000 dans le comté de San Diego (États-Unis) a montré que seulement 14% de la population avait une mauvaise opinion du dessalement[36], des mouvements très actifs se sont formés comme en Australie pour s’opposer à la construction d’usines de dessalement. « J’ai toujours pensé que la minimisation de l’impact sur le milieu marin conditionnerait le développement de la désalinisation. Ce sont les mouvements écologistes qui freinent aujourd’hui plusieurs projets en Californie et en Floride » souligne en 2012 Jean-Michel Herewyn, directeur général de Veolia Water dans une interview au journal Le Monde[37].
C’est un fait que cet aspect est pris très au sérieux dans les projets mais aussi dans les travaux de recherche : nous avons ainsi montré, sur la base d’une étude bibliométrique, que 17% des articles consacrés au dessalement sur la période 1971-2011 font référence à des aspects environnementaux. Qu’en est-il ?
Il est d’abord à noter qu’à une échelle globale, en tenant compte du cycle de l’eau, la salinité ne change pas. L’eau dessalée fini par retourner… à la mer sous forme d’eau usée ou de pluie si elle s’évapore. À l’échelle locale, ça peut être totalement différent.
Les sources de perturbations environnementales ont plusieurs origines. Tout d’abord, on a vu qu’une usine de dessalement rejette une saumure concentrée environ deux fois, à 70 grammes de sel par litre. Le principe adopté est de diluer cette saumure aussi rapidement que possible. Pour les procédés de distillation, cette dilution a lieu dès l’usine en mélangeant la saumure avec l’eau de mer qui sort du condenseur, ce qui permet d’abaisser la concentration à une quarantaine de grammes par litre. Une dispersion en mer termine cette dilution. Pour l’osmose inverse, seule la dispersion en mer permet de diluer la saumure. Un critère courant est que l’accroissement de la salinité doit être inférieur à un gramme par litre à 75 mètres du point de rejet. Beaucoup d’études existent sur les diffuseurs permettant cette dilution. Pour les procédés de distillation, l’eau de mer rejetée est aussi légèrement réchauffée puisqu’elle a servi à condenser de la vapeur et à diluer de la saumure tiède. Cet accroissement de température est limité à quelques degrés au point de rejet et là encore, la dilution limite rapidement la perturbation.
Mais ce n’est pas tout. On a vu que le prétraitement de l’eau de mer qui pénètre dans les usines de dessalement emploie une vaste panoplie de produits chimiques. Une maitrise toujours plus pointue de la conduite des installations permet de limiter au maximum leur usage, dont l’impact économique n’est pas négligeable, et la plus grande partie des réactifs disparait tout simplement, consommée par les réactions chimiques qu’ils provoquent. Toutefois, une concentration résiduelle est rejetée, ce qui a conduit à estimer qu’à cause des usines de dessalement, il est rejeté chaque jour dans le golfe arabique 65 tonnes d’antitartre, 24 tonnes de chlore résiduel et 300 kilogrammes de cuivre issu des produits de corrosion[38]
9. Marché et aspect économique du dessalement des eaux
Les impacts environnementaux mentionnés précédemment n’ont jusqu’à présent pas entamé la dynamique du marché du dessalement de l’eau ; ils pèsent peu face aux besoins et à la diminution des coûts obtenue (tableau 2 en annexe). Dans les cas standards, ces derniers se décomposent en 1/3 pour l’énergie, 1/3 pour l’investissement et 1/3 pour le fonctionnement pour les procédés à osmose inverse. Dans le cas de la distillation, c’est plutôt 40 , 30 et 30 %.
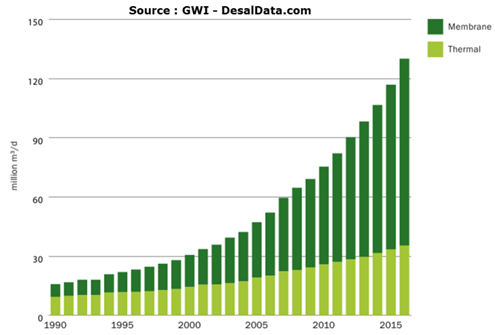
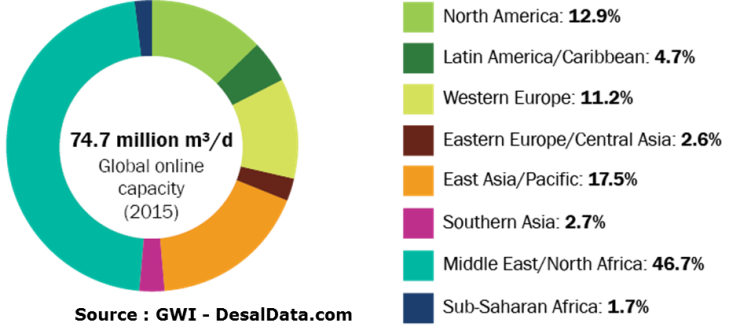
Le cumul de la capacité des usines de dessalement qui ont été installées dans le monde montre une croissance continue depuis près de 30 ans pour dépasser aujourd’hui 100 millions de mètres cubes par jour pour plus de 17 000 installations (les petites unités et celles embarquées sur les navires ne sont pas prises en compte) (Figure 29). Si on ne considère que les installations en service (figure 30), la capacité de production journalière est de 75 millions de mètres cubes[39]. Ce chiffre englobe l’eau produite à partir de la mer et des eaux saumâtres. Néanmoins, ce volume reste bas comparé à la consommation mondiale d’eau dont il ne représente qu’environ 1%.
La capacité installée progresse d’environ 10% par an. Sans surprise les pays du Golfe, du Moyen-Orient et d’Afrique du Nord concentrent la majeure partie de la capacité de production – près de 50%. Plus surprenant, l’Amérique du Nord représente 13% de la capacité mondiale : les États-Unis dessalent beaucoup d’eau saumâtre par osmose inverse dans les états du sud-ouest particulièrement arides. L’Europe de l’Ouest – Espagne, Grèce, Italie – déjà frappée par le manque d’eau a recours au dessalement pour approvisionner ses iles mais aussi de grandes métropoles telles que Barcelone qui possède une usine produisant 200 000 mètres cubes par jour par osmose inverse.
La plus grosse usine de dessalement actuellement en service est celle de Ras Al Khair en Arabie Saoudite qui produit 728 000 mètres cubes par jour dans huit lignes multiflash (MSF) et 17 lignes d’osmose inverse. Elle est couplée à une centrale électrique qui fournit à la fois l’électricité et la chaleur nécessaires au fonctionnement des deux procédés de dessalement. C’est ce qu’on appelle une installation hybride.
Par le procédé d’osmose inverse, la plus grosse capacité aujourd’hui en service est l’usine de Sorek en Israël. Construite par IDE Technologies (Israel Desalination Enterprises), elle produit 627 000 mètres cubes par jour, ce qui porte à 50% la part de l’eau consommée en Israël provenant du dessalement[40] . Le prix de revient de l’eau produite est seulement de 0,58 US$ par mètre cube.
Inversement, il existe de tout-petits équipements de dessalement destinés à la plaisance, à la production domestique ou aux équipements de secours. Leur capacité qui ne dépasse pas quelques litres par jour permet de couvrir le strict nécessaire. Ils fonctionnent éventuellement à l’énergie solaire comme le Water cone de Mage (Figures 31 et 32).
Les acteurs présents sur le marché du dessalement sont multiples. Beaucoup sont présents exclusivement sur le marché de l’osmose inverse dont la croissance est spectaculaire. Ce sont souvent des ensembliers qui achètent les composants – principalement les membranes, pompes et récupérateurs d’énergie – pour fabriquer et livrer des installations clés en mains. D’autres sont présents à la fois sur le marché de l’osmose inverse et sur celui de la distillation.
Très peu ne s’intéressent qu’exclusivement à la distillation sauf dans le cas très particulier des distillateurs embarqués sur les navires et produisant de l’eau à partir de la chaleur récupérée sur le circuit de refroidissement des moteurs.
Du fait de sa maitrise des deux procédés, le groupe français Veolia Water, qui a intégré la société Sidem dans le groupe, est le leader mondial du dessalement en terme de capacité installée. Si on ajoute Degrémont (groupe Suez), la France est largement le premier fournisseur d’usines de dessalement au monde. Parmi les principaux fournisseurs mondiaux, on peut encore citer General Electric Water and Process Technologies (États-Unis), Fisia (Italie), Doosan (Corée), Sasakura (Japon), Hitachi (Japon), IDE (Israël), Alfa Laval (Suède), etc.
10. Conclusion
Avec une capacité journalière de production de 75 millions de mètres cubes par jour en 2015, on peut dire que le dessalement des eaux de mer et saumâtres est une activité industrielle mature. Chaque année, la capacité installée s’accroit de 10%, ce qui représente un marché de plus d’un milliard de dollars. Le coût des usines et de l’eau produite dépend de multiples facteurs et en particulier de celui de l’énergie, thermique et électrique, utilisée pour le dessalement. Pour les grosses installations produisant plusieurs centaines de milliers de mètres cubes par jour, le prix de l’investissement peut descendre en dessous de 1000 dollars par mètre cube par jour tandis que le prix de l’eau produite peut descendre entre 0.5 et 1 dollar le mètre cube.
Si quelques procédés tiennent la quasi-totalité du marché, principalement l’osmose inverse – qui est en très forte progression – et la distillation, la recherche sur de nouvelles méthodes est très active.
Le challenge technique est de mettre au point des procédés toujours plus économes en énergie, si possible renouvelable, en cherchant à se rapprocher de l’ultime limite de l’énergie minimum de dessalement, cela en étant respectueux de l’environnement. L’ambition économique est que l’eau dessalée devienne enfin accessible aux populations pour qui les technologies actuelles restent encore hors de portée pour des questions de coût d’investissement. De ce point de vue, des technologies solaires de petite capacité de production, éventuellement peu performantes mais à très faible coût d’investissement, peuvent tout à fait avoir leur place à côté de l’énorme marché des très grosses usines.
Actualisation d’avril 2023
Le caractère salin, saumâtre ou glacière de la plus grande partie des eaux qui occupent les milliards de km2 de notre planète contraigne à passer par le recyclage et le dessalement pour en permettre l’utilisation. Les techniques assurant une pression osmotique d’au moins 25 bars existent et leur coût ne cesse de décliner. Leur mise en œuvre exigera le recours à l’électronucléaire côtière. Avec ses 5 850 km de côtes, la France est bien placée, sachant que 900 MW en circuit ouvert n’a besoin que d’1 m3/s d’eau pour être refroidi tandis qu’en circuit fermé 2 à 4 m3/s sont évaporés par tours réfrigérantes. Voir André Pellen. Une énergie abondante pour pallier le manque d’eau. Energie et matières premières. 19 avril 2023
11. Annexe
Tableau 2 : Comparaison synthétique des différents procédés de dessalement des eaux
| Procédé* | Énergie thermique
kWh/m3 |
Énergie électrique
kWh/m3 |
Qualité de l’eau**
mg/l |
Investissement dessalement
US$/(m3/j) |
Prix de l’eau
US$/m3 |
| MSF | 70 – 80 | 2,5 – 5 | 10 | 1200 – 2500 | 0,6 – 2 |
| MED | 40 – 65 | 2 – 2,5 | 10 | 900 – 2000 | 0,5 – 1,5 |
| MVC | 0 | 7 – 12 | 10 | 1100 – 3500 | 2 – 2,6 |
| MED-TVC | 50 | 1 – 2 | 10 | 1000 – 2000 | 0,5 – 1 |
| SWRO | 0 | 4 – 6 | 400 – 500 | 900 – 2500 | 0,5 – 2 |
| BWRO | 0 | 1,5 – 2,5 | 200 – 500 | 300 – 1200 | 0,3 – 1,5 |
| ED | 0 | 1,5 – 4 | 150 – 500 | 300 – 400 | 0,6 – 1 |
| Solaire
CSP+MED |
40 – 65 | 2 – 2,5 | 10 | 900 – 2000 | 2,4 – 2,8 |
| Solaire
PV+SWRO |
0 | 4 – 6 | 400 -500 | 900 – 2500 | 12 – 16 |
| Solaire
PV+BWRO |
0 | 1,5 – 2,5 | 200 – 500 | 300 – 1200 | 7 – 9 |
| Solaire
PV/ED |
0 | 1,5 – 4 | 150 – 500 | 300 – 400 | 10 – 12 |
| Eolien SWRO | 0 | 4 – 6 | 400 – 500 | 900 – 2500 | 2 – 10 |
| Eolien BWRO | 0 | 1,5 – 2,5 | 200 – 500 | 300 – 1200 | 1 – 5 |
| Eolien MVC | 0 | 7 – 12 | 10 | 1100 – 3500 | 5 – 8 |
| Géothermie
MED |
40 – 65 | 2 – 2,5 | 10 | 900 – 2000 | 2 – 3 |
Sources : Al-Karaghouli A., Kazmerski L.L. (2012)[41] et Ghaffour N., Missimer T.M., Amy G.L. (2013)[42]
*MSF : Multistage Flash, vaporisation instantanée multi-étagée
MED : Multi-Effect Distillation, distillation multiple-effet
MVC : Mechanical Vapor Compression, compression mécanique de vapeur
MED-TVC : Multi-Effect Distillation-Thermal Vapour Compression, distillation multiple-effet-thermocompression de vapeur
SWRO : Seawater Reverse Osmosis, osmose inverse d’eau de mer
BWRO : Brackish Water Reverse Osmosis, osmose inverse d’eau saumâtre
ED : Electrodialysis, électrodialyse
CSP : Concentrated Solar Power, centrale électrique à solaire concentré (avec cycle de Rankine produisant l’électricité)
PV : photovoltaïque
** Concentration en sel dans l’eau produite. Une seule passe pour l’osmose inverse
Notes et références
[1] World Health Organisation (2015) Progress on sanitation and drinking water, 2015 update and MDG assessment, 90p Disponible sur http://apps.who.int/iris/bitstream/10665/177752/1/9789241509145_eng.pdf?ua=1
[Consulté le 2/10/2016]
[2] Nations-Unies (2006) L’eau, une responsabilité partagée [2ème Rapport mondial des Nations Unies sur la mise en valeur des ressources en eau UN-WATER/WWAP/2006/3] Disponible en anglais et résumé en français sur
[Consulté le 02/10/2016]
[3] Howard Guy, Bartram Jamie (2003), Domestic Water Quantity, Service Level and Health, World Health Organization, 33p. Disponible sur http://www.who.int/water_sanitation_health/diseases/WSH03.02.pdf [Consulté le 07/11/2016]
[4] Ces raisons sont identifiées dans les différents rapports WWAP (World Water Assessment Programme) des Nations-Unies disponibles sur http://www.unesco.org/new/en/natural-sciences/environment/water/wwap/wwdr/ et synthétisées p. 7 du rapport de Cosgrove Catherine E. and Cosgrove William J. (2012). The Dynamics of Global Water Futures Driving Forces 2011–2050. Paris: UNESCO, 94p [Report on the findings of Phase One of the UNESCO-WWAP – Water Scenarios Project to 2050] Disponible sur
http://unesdoc.unesco.org/images/0021/002153/215377e.pdf [Consulté le 02/10/2016]
[5] Selon le rapport WWAP (2009), la croissance rapide de la population a conduit à un triplement des prélèvements en eau sur les cinquante dernières années. WWAP (2009), World Water Development Report3: Water in a Changing World – Facts and Figures. p8. Paris: UNESCO. Disponible sur http://www.unesco.org/new/en/natural-sciences/environment/water/wwap/wwdr/wwdr3-2009/ [Consulté le 02/10/2016]
[6] CNRS. Dossier scientifique : l’eau. Disponible sur : http://www.cnrs.fr/cw/dossiers/doseau/decouv/cycle/stocksEau.html [Consulté le 07/11/2016]
[7] Calcul propre effectué à partir des données de population en zone côtière en 2010 issues du Center for International Earth Science Information Network – CIESIN – Columbia University (2012). National Aggregates of Geospatial Data Collection: Population, Landscape, And Climate Estimates, Version 3 (PLACE III). Palisades, NY: NASA Socioeconomic Data and Applications Center (SEDAC) Disponibles sur http://dx.doi.org/10.7927/H4F769GP [Consulté le 07/11/2016] et de la donnée de population mondiale en 2010 des Nations-Unies, soit 6 929 725 043 habitants. Source : United Nations (2015) Department of Economic and Social Affairs, Population Division, World Population Prospects: The 2015 Revision, (DVD Edition) Disponible sur: https://esa.un.org/unpd/wpp/Download/Standard/Population/ [Consulté le 07/11/2016]
[8] James D. Birkett (2012). The History of Desalination Before Large-Scale Use, in Desalination and Water Resources – History, Development and Management of Water Resources,Vol.I. Paris: Unesco. pp.381-434 I (Encyclopedia of life support systems)
[9] S. Loeb (1981). The Loeb-Sourirajan Membrane: How It Came About, in Turbak A.F. Synthetic membranes. Washington, DC : American Chemical Society. 9p. (ACS Symposium Series). doi: 10.1021/bk-1981-0153.ch001. Disponible sur : http://pubs.acs.org/doi/pdfplus/10.1021/bk-1981-0153.ch001?src=recsys [Consulté le 23/11/ 2016]
[10] Cité par : Pastor Jean, Pauli Anne-Marie (1995). Dialyse. Chromatographie et techniques séparatives. Paris : Techniques de l’Ingénieur – p 1525. Disponible sur : http://www.techniques-ingenieur.fr/base-documentaire/mesures-analyses-th1/chromatographie-et-techniques-separatives-42385210/dialyse-p1525/ [Consulté le 23/11/2016]
[11] RUMEAU Michel. Membranes, transferts. Encyclopædia Universalis. Disponible sur : http://www.universalis.fr/encyclopedie/membranes-transferts/ [Consulté le 23/11/2016]
[12] Pour un coût du kWh bois de 0,04 € TTC (donnée 2015, consommateurs domestiques en France) et du kWh électrique de 0,15 € hors TVA (donnée 2015 EUROSTAT, tarif industriel européen le plus élevé). Source : Commissariat général au Développement durable, Observation et statistiques, prix des énergies. Disponible sur http://www.statistiques.developpement-durable.gouv.fr/energie-climat/r/prix-energies.html?tx_ttnews%5Btt_news%5D=23473&cHash=998f1a70b7e362103a6872b902a95f70 [Consulté le 23/11/2016]
[13] A titre de comparaison, au robinet, on paie en France en 2016 entre 3 et 6 €/m3, tout compris (fourniture d’eau et assainissement). La part de « production » (puisage, potabilisation et transport) en représente moins de la moitié. Source : Observatoire National des Services d’Eau et d’Assainissement. Disponible sur : http://www.services.eaufrance.fr/
[14] Comme par exemple celles de Laboceano, Laboratoire brésilien de technologie océanique : http://www.laboceano.coppe.ufrj.br/ittc2011/documents/2011/pdf Procedures 2011/7.5-02-01-03.pdf
[Consulté le 04/11/2016]
[15] M. Rochon (1813). Mémoire sur l’épuration de l’eau de mer, rendue potable sans goût d’empyreume, par distillation dans le vide, Journal de Physique, de Chimie et d’histoire naturelle et des arts, Vol.76, p. 373
[16] La pression de saturation est la pression qui assure l’équilibre liquide-vapeur à température donnée (en rouge sur la figure 8)
[17] Mahmoud Abdel-Jawad (2001). Energy sources for coupling with desalination plants in the GCC countries. (consultancy report prepared for ESCWA)
[18] Wangnick (2004), IDA Worldwide Desalting Plants Inventory, Report n°18. Wangnick Consulting GmbH, Germany
[19] http://www.energyrecovery.com/water/px-pressure-exchanger/ [Consulté le 04/11/2016]
[20] M. Abdel-Jawad (2001).op cit
[21] Ben Aïm R. (2009). Les nouvelles séparations membranaires, Paris : Journées Techniques SF2P, 5 nov, Disponible sur : http://sf2p.separation.free.fr/PdF/P3-Benaim.pdf [Consulté le 04/11/2016]
[22] Kullab A., Martin A.(2011). Membrane distillation and applications for water purification in thermal cogeneration plants, Sep. Purif. Technol., Vol.76, pp. 231–237.
[23] Mazlan N. M. et al. (2016). Energy consumption for desalination – A comparison of forward osmosis with reverse osmosis, and the potential for perfect membranes. Desalination, vol. 377, pp.138–151
[24] Davison et al. R. (1960) Structure and amine-water solubility in desalination by solvent extraction. Journal of Chemical Engineering Data, vol. 5, n°4.
[25] TMW, Mage Water Management, Altela, Terrawater
[26] Atlantis™ , http://www.atlantis-water.com/
[27] Institut für Chemische Verfahrenstechnik (2009) Electromembrane processes: state-of-the-art processes and recent developments, Univ. Stuttgart, Disponible sur: https://ocw.mit.edu/courses/mechanical-engineering/2-500-desalination-and-water-purification-spring-2009/readings/MIT2_500s09_read12.pdf [Consulté le 23/11/2016]
[28] Saltworks Technologies, http://www.saltworkstech.com
[29] Kim Sung Jae et al. (2012). A portable and high energy efficient desalination/purification system by ion concentration polarization. Nanosystems in Engineering and Medicine, Proc. of SPIE 2012, Vol. 8548 85483R-1, Disponible sur: http://dx.doi.org/10.1117/12.2000052 [Consulté le 07/11/2016]
[30] Höpfner J. (2013). A new method of seawater desalination via acrylic acid based hydrogels, Karlsruher Institut für Technologie (KIT) (Dissertation) Disponible sur : http://www.ksp.kit.edu/9783731501435 [Consulté le 07/11/2016]
[31] Jitendra S. Sangwai and al. (2013) Desalination of seawater using gas hydrate technology – Current status and future direction, IIT Madras, Chennai, India (Proceedings of Hydro 2013 International, 4-6 Dec) Disponible sur: https://www.researchgate.net/publication/259266834_DESALINATION_OF_SEAWATER_USING_GAS_HYDRATE_TECHNOLOGY_-_CURRENT_STATUS_AND_FUTURE_DIRECTION [Consulté le 04/11/2016]
[32] Arámburo-Miranda A.V. et al. (2014). Desalination of sea water with aquatic lily (Eichhornia crassipes). 4th Int. Symp. on Environmental Biotech. and Eng. DOI 10.1007/s11356-016-7160-9
[33] Clus O. (2007). Condenseurs radiatifs de la vapeur d’eau atmosphériques (rosée) comme source alternative d’eau douce, thèse de l’Université de Corse.
[34] Eole Water, http://www.eolewater.com/fr/index.html [Consulté le 04/11/2016]
[35] Ozden S. and al. (2014). Anisotropically functionalized carbon nanotube array based hygroscopic scaffolds, Applied Materials and Interfaces, vol. 6, pp. 10608−10613, dx.doi.org/10.1021/am5022717
[36] Bleninger T., Jirka G. H. (2010). Environmental planning, prediction and management of brine discharges from desalination plants, Middle East Desalination Research Center, MEDRC (Series of R&D Reports, MEDRC Project: 07-AS-003)
[37] Valo M. (2012). Dessaler l’eau de mer : un remède au manque d’eau ? Cent cinquante pays disposent d’infrastructures de désalinisation. Mais les techniques restent chères et énergivores, Le Monde, 18 Avril.
[38] Bleninger T., Jirka G.H. (2010), op cit.
[39] Global Water Intelligence, DesalData (2016), https://www.globalwaterintel.com/ [Consulté le 04/11/2016, site accessible sur abonnement]
[40] D. Talbot, Megascale Desalination, MIT Technology Review, 2015
https://www.technologyreview.com/s/534996/megascale-desalination/ [Consulté le 04/11/2016]
[41] Al-Karaghouli A., Kazmerski L. (2012). Comparisons of technical and economic performance of the main desalination processes with and without renewable energy coupling, Denver, Colorado : National Renewable Energy Laboratory, p.13-17 (World Renewable Energy Forum 2012) Disponible sur https://ases.conference-services.net/resources/252/2859/pres/SOLAR2012_0591_presentation.pdf [Consulté le 02/11/2016]
[42] Ghaffour N., Missimer T. M., Amy G. L. (2013). Technical review and evaluation of the economics of water desalination: Current and future challenges for better water supply sustainability, Desalination, vol. 309, January, pp 197-207.
Bibliographie complémentaire
http://www.desline.com/
http://www.edsoc.com/
http://www.ide-tech.com/
http://idadesal.org/
http://www.medrc.org/
http://www.veoliawatertechnologies.com/fr/dessalement
L’Encyclopédie de l’Énergie est publiée par l’Association des Encyclopédies de l’Environnement et de l’Énergie (www.a3e.fr), contractuellement liée à l’université Grenoble Alpes et à Grenoble INP, et parrainée par l’Académie des sciences.
Pour citer cet article, merci de mentionner le nom de l’auteur, le titre de l’article et son URL sur le site de l’Encyclopédie de l’Énergie.
Les articles de l’Encyclopédie de l’Énergie sont mis à disposition selon les termes de la licence Creative Commons Attribution – Pas d’Utilisation Commerciale – Pas de Modification 4.0 International.




![Fig. 2 : Production d’eau douce par condensation sur une éponge - Source : Howarth, 1984. Voir réf. [8]](https://www.encyclopedie-energie.org/wp-content/uploads/2016/11/art121_figure2_Production-eau-douce-condensation-eponge.png)